在创新药产业快速发展,以及打造科研型医院的政策驱动下,临床研究需求不断攀升,临床试验机构资源吃紧,药物临床试验机构备案制度发布,让更多具备能力的医疗机构有机会开展临床试验。
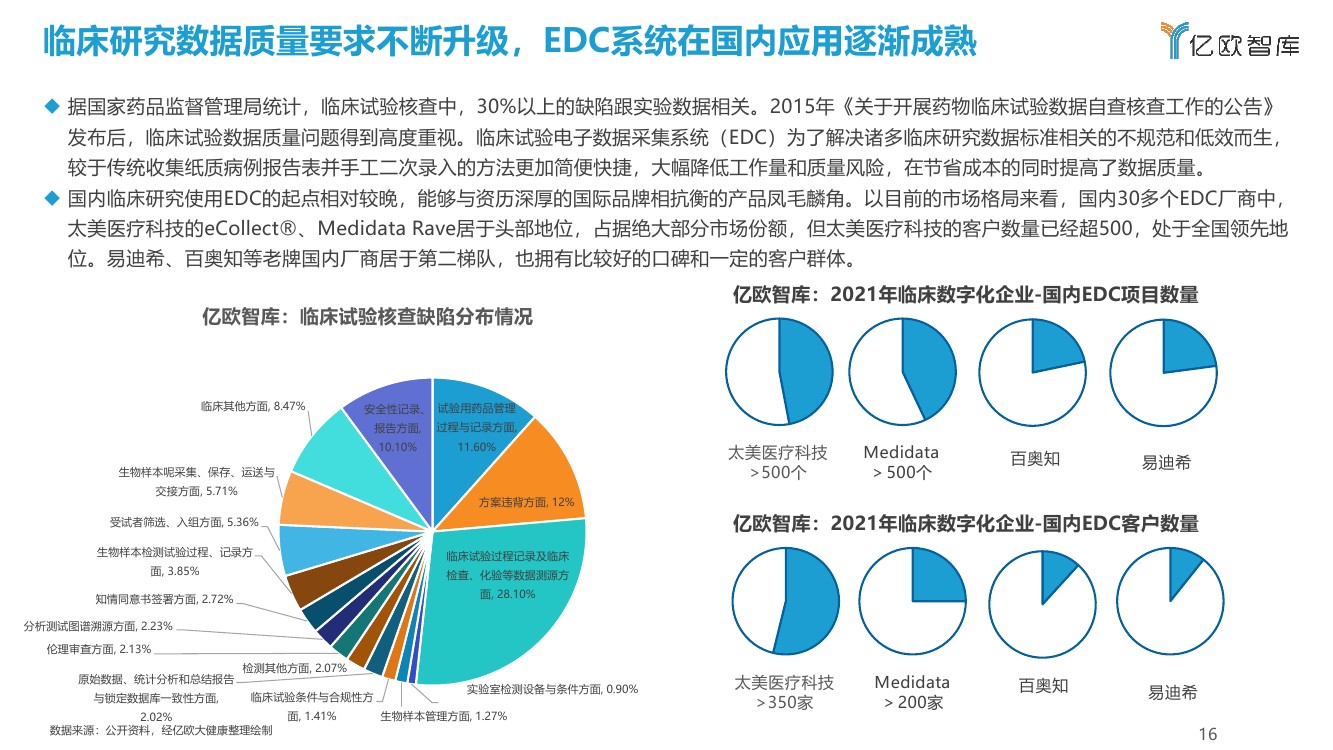
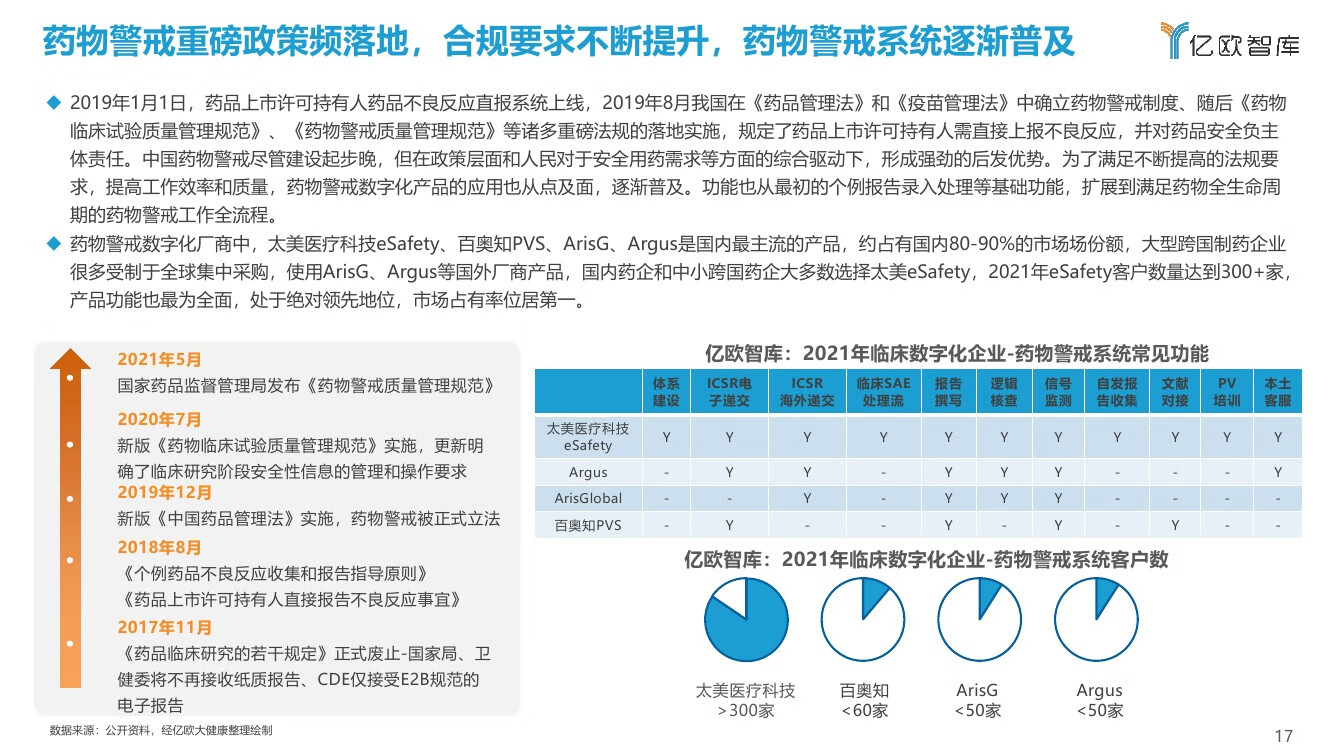
在2015年之前,临床研究数据多以纸质文件记录。2015年7月,随着国家食药监局发布《关于开展药物临床试验数据自查核查工作的公告》(2015年第117号)》,此次《公告》号称“史上最严的数据核查要求”,企业开始纷纷注重数据的合规性,临床研究数字化系统被逐渐开始普及使用。
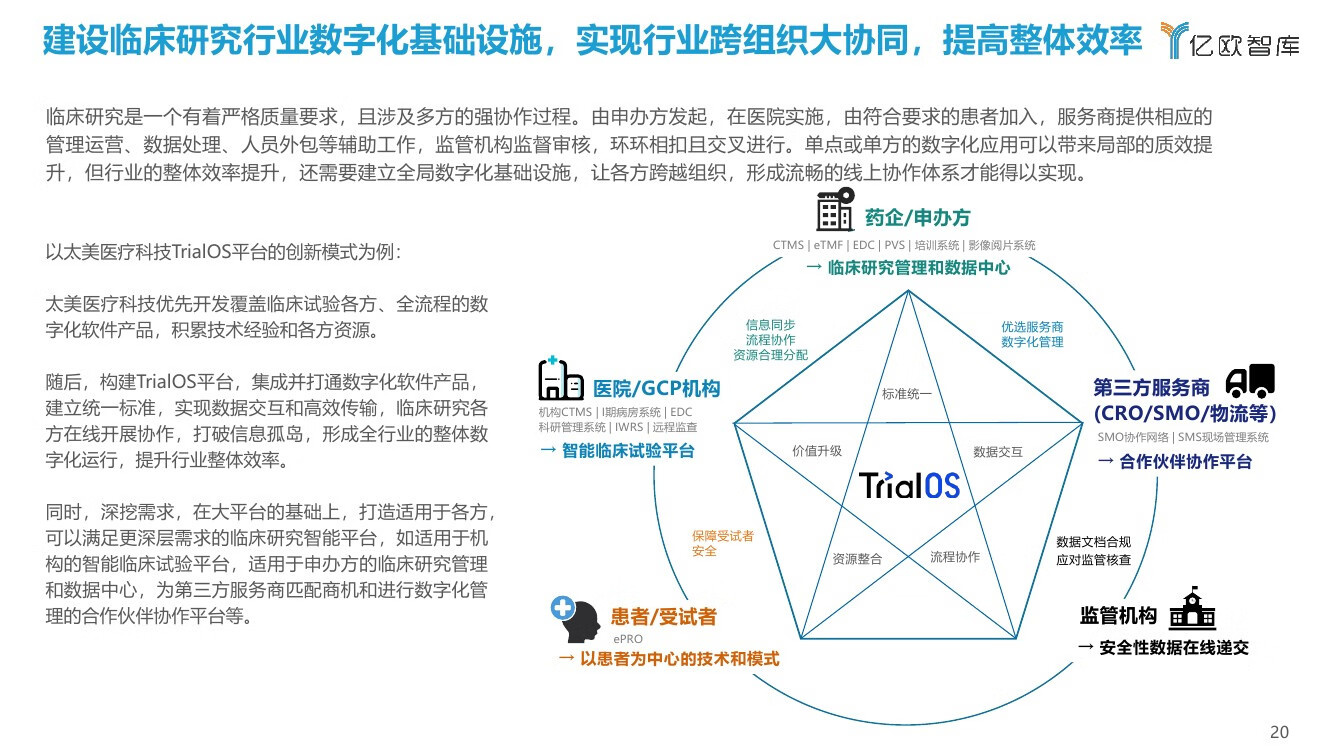
2015年左右,随着云计算技术的成熟和在临床研究领域的深化应用,更加灵活地部署及软件形式,帮助临床数字化在可操作性及便捷性上有了新的突破,也成为了临床研究领域进入智能平台时代的坚定基石。
报告内容
本报告发布时间20211227
本报告共52页,内容如下:


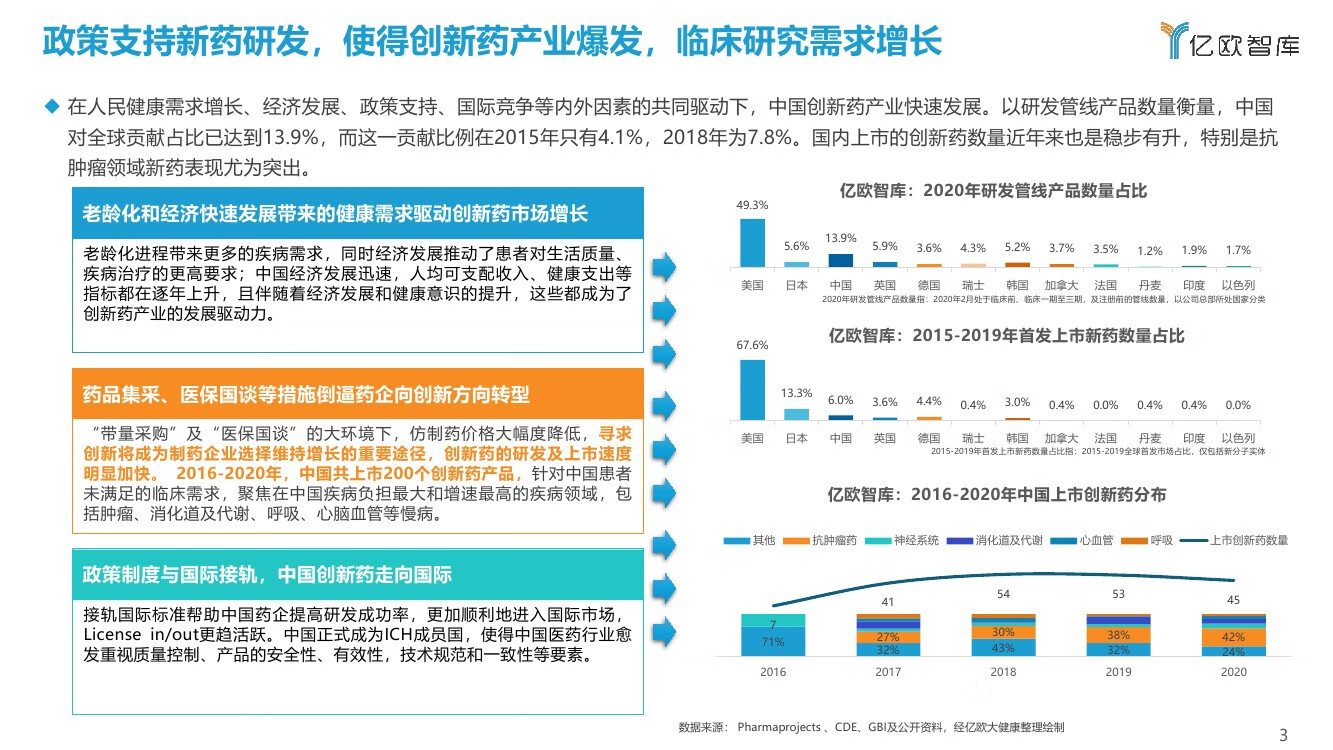
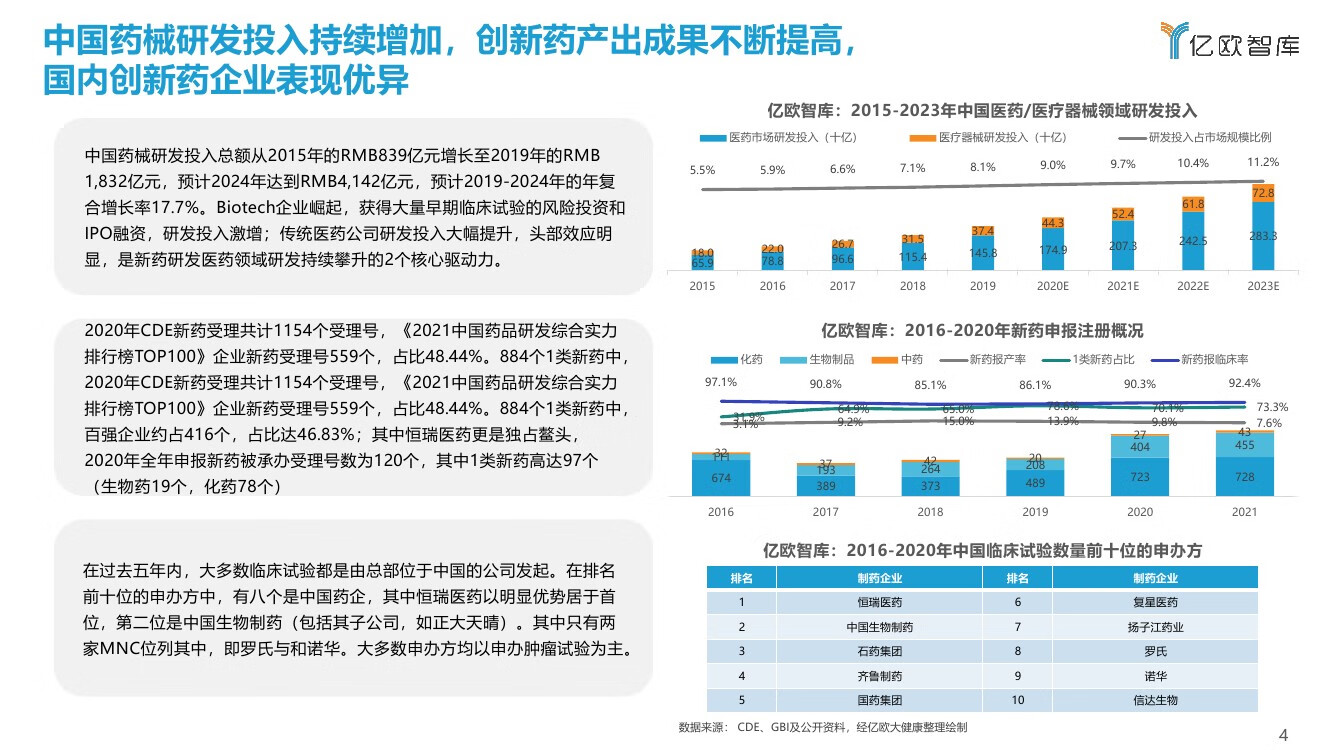
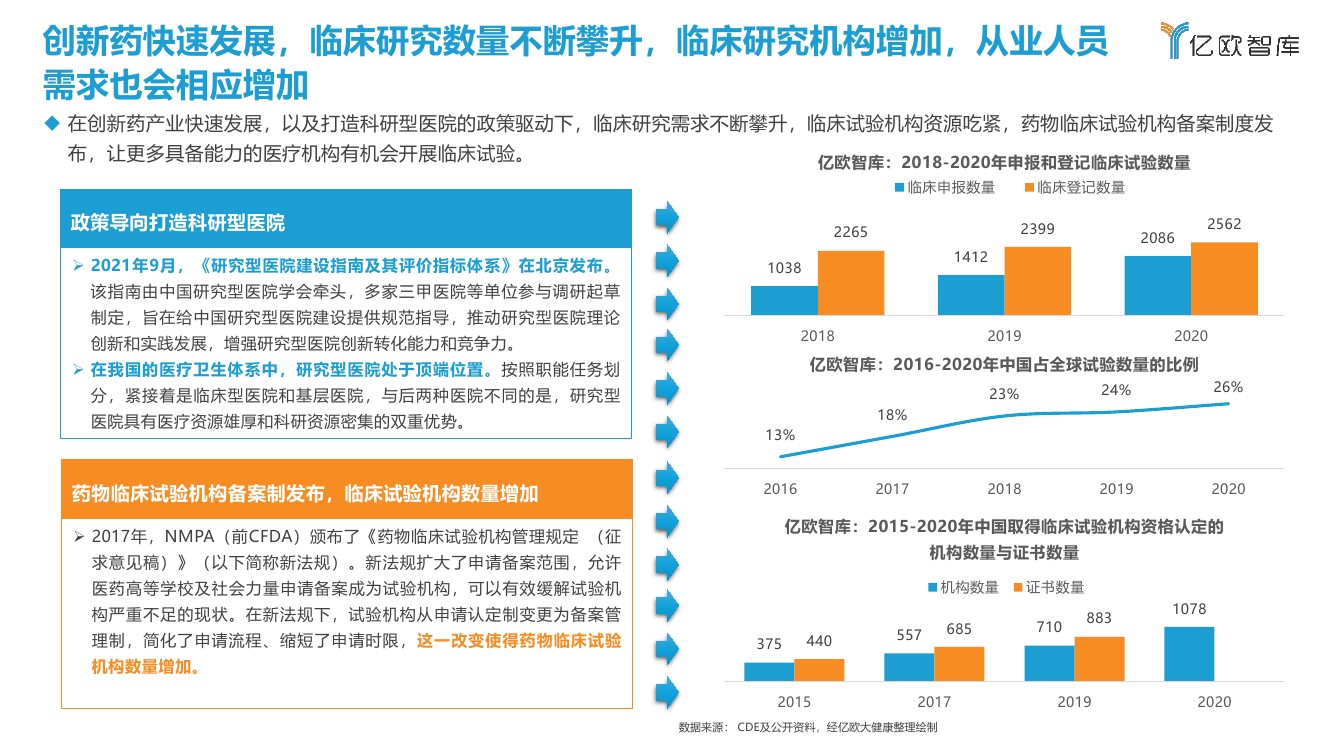

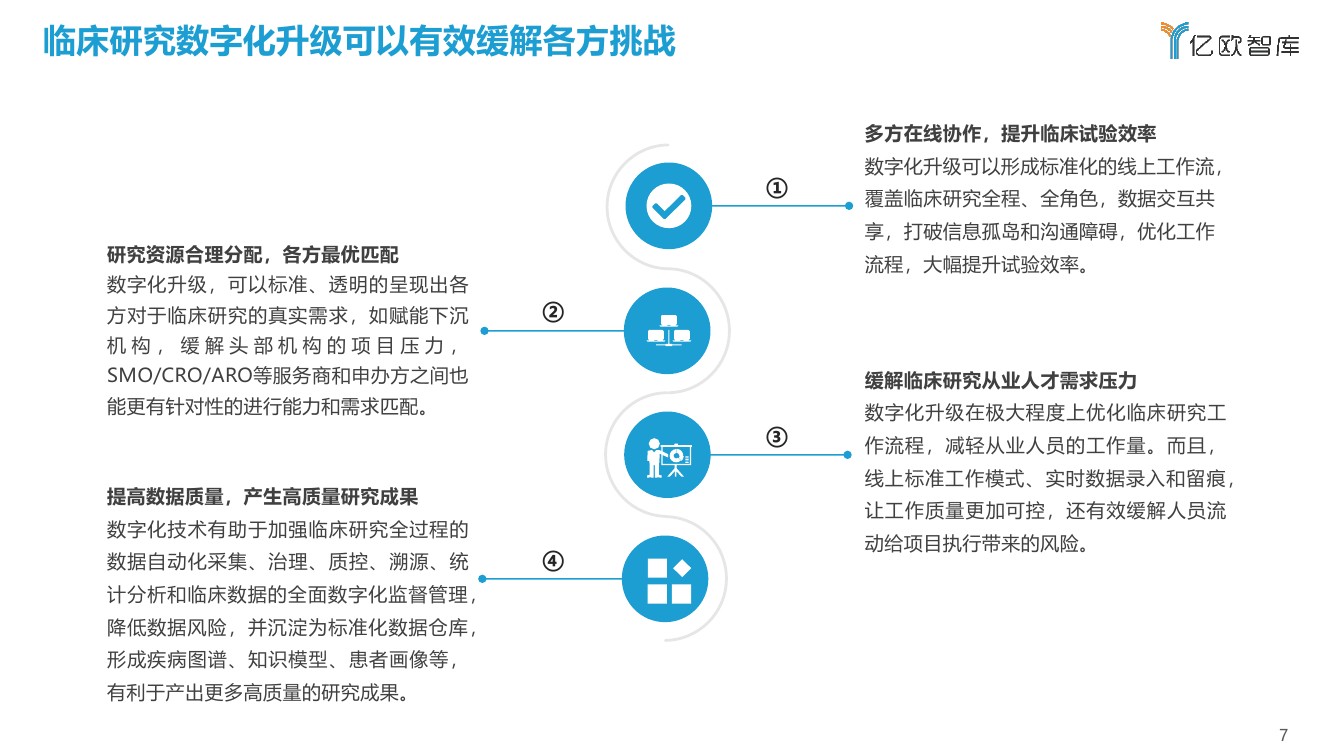





★篇幅限制,仅显示部分内容
下载完整报告
您暂时无权查看此 隐藏内容!可付费查看





 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏
